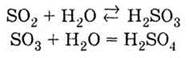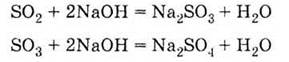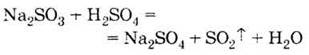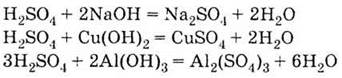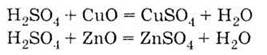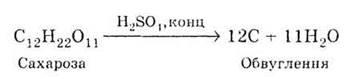Хімія - універсальний довідник
ХІМІЯ НЕМЕТАЛІЧНИХ ЕЛЕМЕНТІВ
СУЛЬФАТНА КИСЛОТА ТА ЇЇ СОЛІ
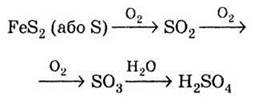
У творений при окисненні діоксиду сульфуру триоксид сульфуру — кислотний оксид. Під час його взаємодії з водою утворюється сульфатна кислота Н2SO4:
![]()
Безводна сульфатна кислота — рідина, густина якої майже у два рази перевищує густину води. Вона змішується з водою у будь-яких пропорціях. Процес розчинення супроводжується виділенням великої кількості тепла, що свідчить про утворення з водою хімічних сполук.
Сульфатна кислота, яка постачається споживачеві, має концентрацію близько 95% і густину ρ = 1,83 г/см3.
У розбавлених розчинах сульфатна кислота виявляє усі типові властивості кислот. Вона забарвлює у відповідний колір індикатори, дисоціюючи з утворенням іонів Гідрогену:
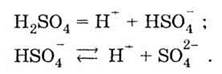
При цьому по першому щаблеві сульфатна кислота дисоціює необоротно, а по другому — оборотно.
Сульфатна кислота взаємодіє з металами, які стоять у ряді напруг лівіше Гідрогену, з основними оксидами, з основами, а також із солями, наприклад:
![]()
У таблиці на с. 42 узагальнено хімічні властивості сірки та її сполук.
Таблиця
Сірка та її сполуки
|
Сполуки cульфуру |
||
оксиди сульфуру |
сульфатна кислота |
|
1. За звичайних умов — жовта кристалічна речовина. 2. Горить у кисні:
(проявляє відновні властивості) 3. Взаємодіє з металами і воднем:
(проявляє окисні властивості) У природі зустрічається самородна сірка S, сульфіди FеS2 (пірит), СuS; сульфати СаSО1 • 2Н20 (гіпс), Nа2 SO4 |
1. За звичайних умов SO2 — газ, SO3 — тверда речовина 2. Проявляють властивості кислотних оксидів, взаємодіючи з водою:
з лугами:
з основними оксидами:
Одержання 1) оксиду сульфуру (IV) у промисловості: горіння сірки
випалювання піриту
в лабораторії:
2) оксиду сульфуру (VI) у промисловості: каталітичне окиснення оксиду сульфуру (IV)
|
1. За звичайних умов безбарвна важка (ρ ≈ 2 г/см) рідина, необмежено розчинна у воді 2. Сильна двохосновна кислота:
3. Взаємодіє з металами:
Концентрована кислота пасивує Аl і Fе 4. Взаємодіє з лугами, основами і амфотерними гідроксидами:
5. Взаємодіє з основними і амфотерними оксидами:
6. Концентрована кислота гігроскопічна:
Одержання у промисловості:
|
Перша публікація: 01/01/2008
Останнє оновлення: 31/12/2023
Редакційна та навчальна адаптація: Даний матеріал зведено на основі першоджерела/оригінального тексту. Команда проєкту здійснила редакційне оглядове опрацювання, виправлення технічних неточностей, структурування розділів та адаптацію змісту до навчального формату.
Що було опрацьовано:
- усунення форматних дефектів (OCR-помилки, розриви структури, дефектні символи);
- редакційне упорядкування змісту;
- уніфікація термінів відповідно до академічних джерел;
- перевірка відповідності фактичних тверджень тексту першоджерела.
Усі згадки про автора, рік видання та походження первинного тексту збережено відповідно до джерела.