Хімія - універсальний довідник
ХІМІЧНИЙ ПРОЦЕС
ТЕРМОДИНАМІКА ХІМІЧНОГО ПРОЦЕСУ
ТЕПЛОВИЙ ЕФЕКТ РЕАКЦІЇ. ЕНТАЛЬПІЯ РЕАКЦІЇ
Кількість теплоти Q, яку передали системі, йде на зміну її внутрішньої енергії ΔUі на здійснення системою роботи* W проти зовнішніх сил (зовнішнього тиску р) (рис. 32):
![]()
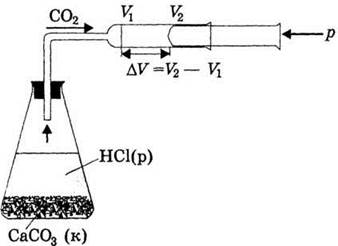
Рис. 32. Робота, яку виконує хімічна система проти зовнішнього тиску (поршень невагомий).
Вуглекислий газ, який виділяється при взаємодії карбонату кальцію із хлоридною кислотою, тисне на поршень і зрушує його на величину ΔV:
Під час ізохорного процесу (ΔV = 0, W = 0) тепловий ефект реакції визначається зміною внутрішньої енергії системи ΔU:
![]()
Під час ізобарного процесу тепловий ефект реакції визначається зміною ентальпії системи ΔH:
![]()
Якщо реакція екзотермічна (зменшення енергії системи ΔН < 0 (рис. 33); якщо реакція ендотермічна (збільшення енергії системи), ΔН > 0 (рис. 34).
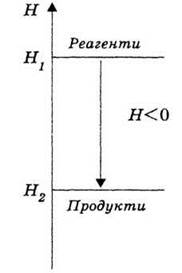
Рис. 33. Зміна ентальпії системи в екзотермічній реакції.
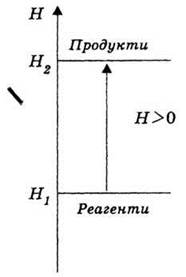
Рис. 34. Зміна ентальпії системи в ендотермічній реакції.
* Роботу позначають символом W замість символу А.
Перша публікація: 01/01/2008
Останнє оновлення: 31/12/2023
Редакційна та навчальна адаптація: Даний матеріал зведено на основі першоджерела/оригінального тексту. Команда проєкту здійснила редакційне оглядове опрацювання, виправлення технічних неточностей, структурування розділів та адаптацію змісту до навчального формату.
Що було опрацьовано:
- усунення форматних дефектів (OCR-помилки, розриви структури, дефектні символи);
- редакційне упорядкування змісту;
- уніфікація термінів відповідно до академічних джерел;
- перевірка відповідності фактичних тверджень тексту першоджерела.
Усі згадки про автора, рік видання та походження первинного тексту збережено відповідно до джерела.